Morphosys hat im vergangenen Jahr mit Tremfya (Guselkumab) die erste Zulassung in der Firmengeschichte gefeiert. Tremfya ist ein mithilfe von Morphosys‘ Antikörpertechnologie HuCAL erzeugter, vollständig humaner monoklonaler Antikörper, der gegen IL-23 gerichtet ist und von Janssen entwickelt wird. Bislang war das Mittel zur Behandlung von Schuppenflechte bereits in den USA, Kanada und der Europäischen Union zugelassen. Zuletzt gaben auch einige andere Länder grünes Licht: Auf Brasilien und Australien folgte Japan. Nun gab Morphosys bekannt, dass eine Tochterfirma des Lizenzpartners, Janssen Korea Ltd. (Janssen) gemeldet hat, dass nun auch das südkoreanische Ministerium für Lebensmittel- und Arzneimittelsicherheit Tremfya für die Behandlung von erwachsenen Patienten mit mittelschwerer bis schwerer Plaque-Psoriasis (Schuppenflechte) zugelassen hat, bei denen eine Phototherapie oder systemische Therapie erforderlich ist.
Morphosys ist über Tantiemen an den Umsatzerlösen von Tremfya beteiligt. Neben Psoriasis wird Tremfya derzeit in einem Phase-3-Entwicklungsprogramm bei Patienten mit psoriatischer Arthritis untersucht. Janssen hat zudem angekündigt, Guselkumab auch in der Indikation Morbus Crohn prüfen zu wollen. Hier kann man in den kommenden Monaten auf weitere Daten gespannt sein – wie auch bei einer Vielzahl von weiteren Projekten. Der Fokus liegt bei Morphosys derzeit aber klar auf dem am weitesten fortgeschrittenen eigenen Projekt MOR208. Hier könnte, wenn alles gut läuft, in zwei Jahren der Marktstart erfolgen.
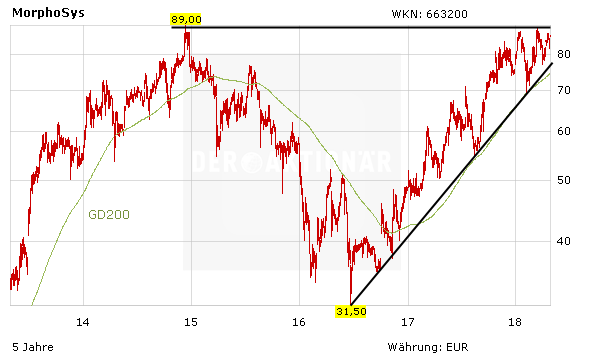
Die Morphosys-Aktie gewinnt am Freitagmorgen knapp ein Prozent auf 85,50 Euro und nähert sich damit erneut dem wichtigen Widerstand in Form des Mehrjahreshochs bei 89 Euro. Es dürfte nur noch eine Frage der Zeit sein, bis der Ausbruch nach oben gelingt. Morphosys bleibt einer der besten deutschen Biotechwerte.

 DER AKTIONÄR – Unsere App
DER AKTIONÄR – Unsere App


 27.04.2018
27.04.2018


 Sofortkauf
Sofortkauf

